Исследователи выявили связь образованности и смертности
Об этом гласит их статья , размещенная в The Lancet Public Health. Учеными были изучены данные свыше научных публикаций, где рассматривается связь уровня образования с длительностью жизни человека. Отмечается, что специалистами были исследованы статьи из 59 государств, в числе которых как промышленно развитые, например, США или страны ЕС, так и развивающиеся, в частности, Китай, Бразилия и многие другие. Перейти на мобильную версию.

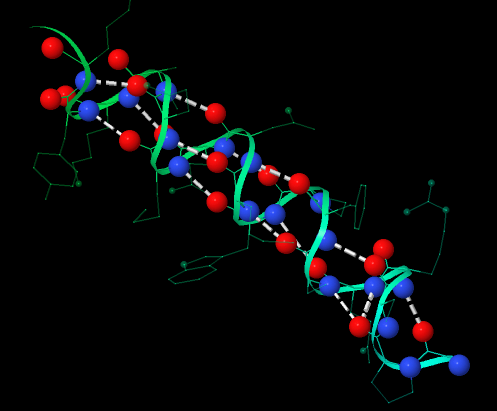



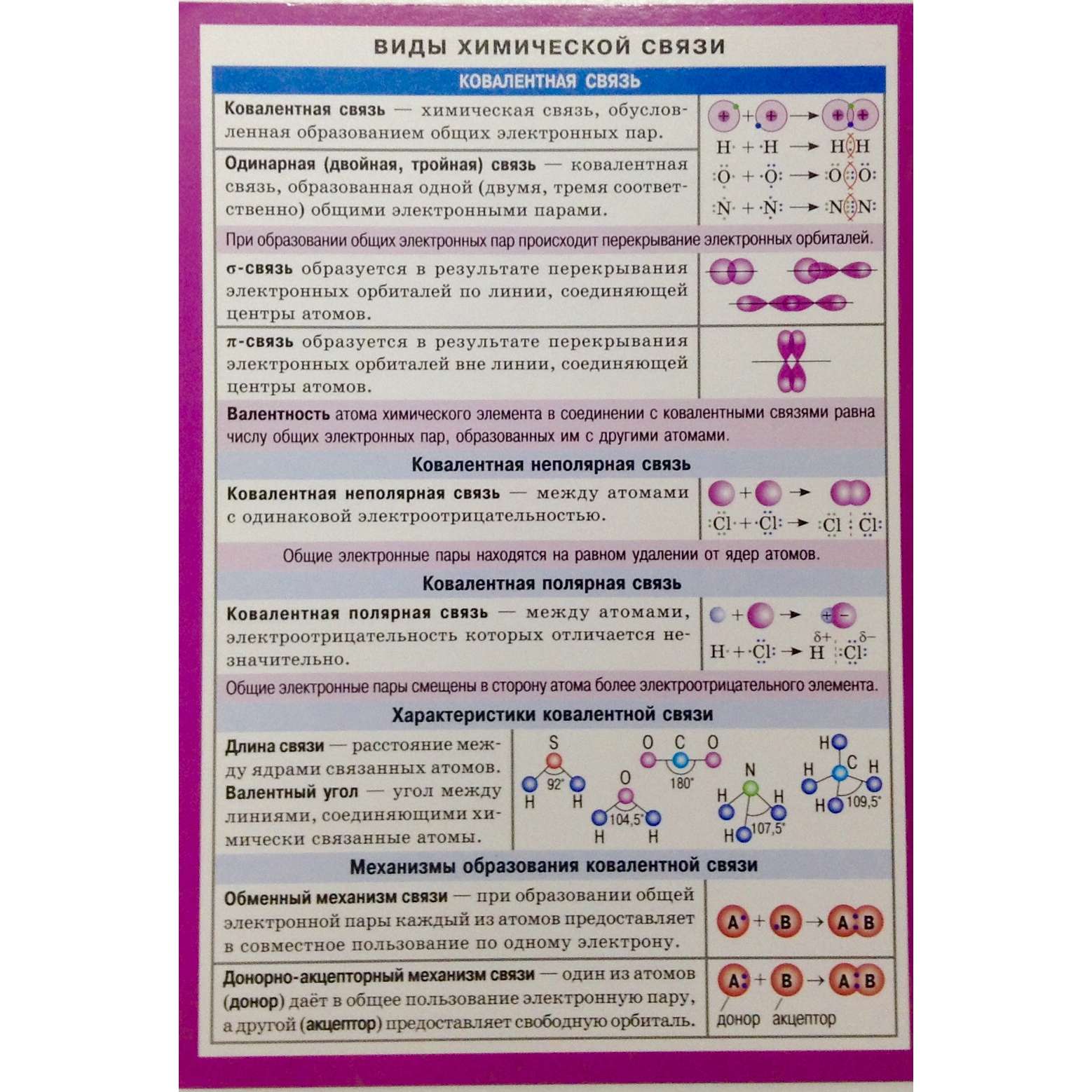
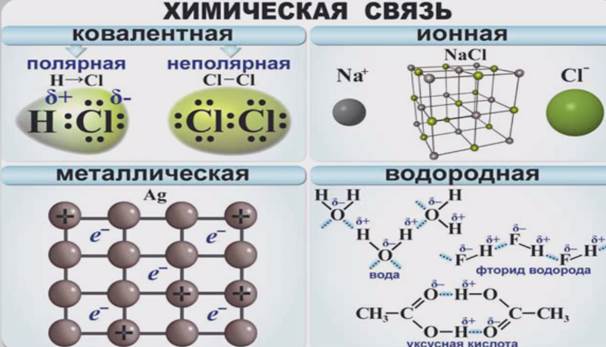
Идеальная ионная связь отвечает образованию в соединении разноименно заряженных ионов за счёт смещения электронной плотности между атомами, как если бы произошёл перенос электрона ов от атома с меньшей электроотрицательностью к атому с большей электроотрицательностью с образованием катиона и аниона , между которыми действует сила электростатического притяжения. Таким образом, ионная связь может рассматриваться в качестве крайнего случая при поляризации ковалентной связи. Характерна для бинарных соединений металлов и неметаллов и других солей. Энергия ионной связи и взаимное расположение ионов в соединении определяется электростатическим взаимодействием между ионами, в которых распределение заряда перестаёт быть сферическим и становится ориентированным в соответствии с поляризацией, которую оказывают соседние ионы. Большинство соединений с ионной связью имеют твердое агрегатное состояние при нормальных условиях [2] [1] [3]. На практике, идеальной ионной связи не существует, и более корректно говорить об ионном характере химической связи либо о ее полярности, которые могут также выражаться в степени переноса заряда между атомами или в их эффективных зарядах [2].
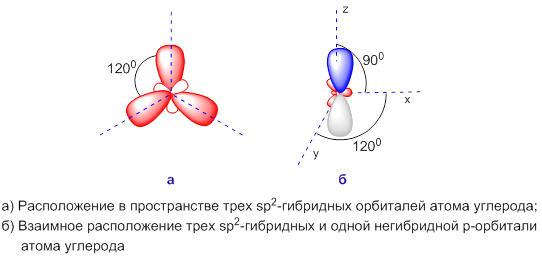
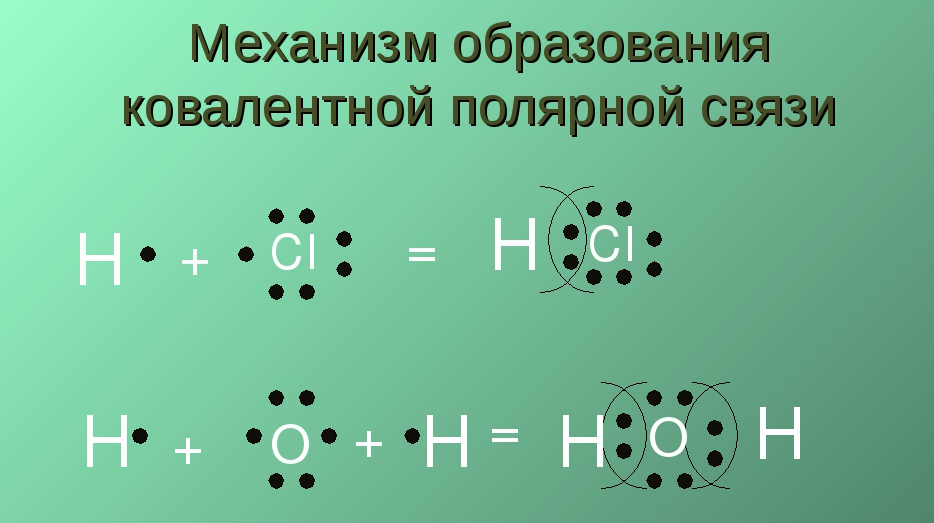
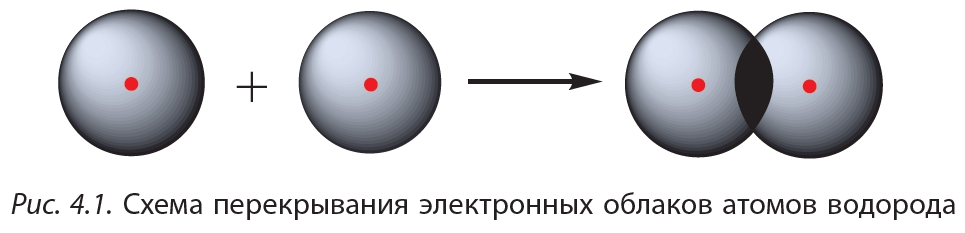
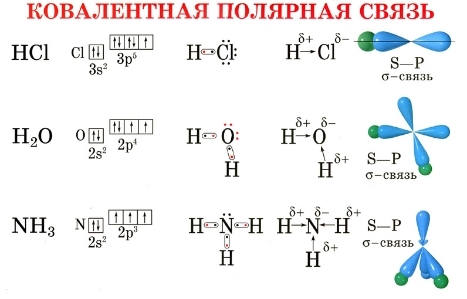
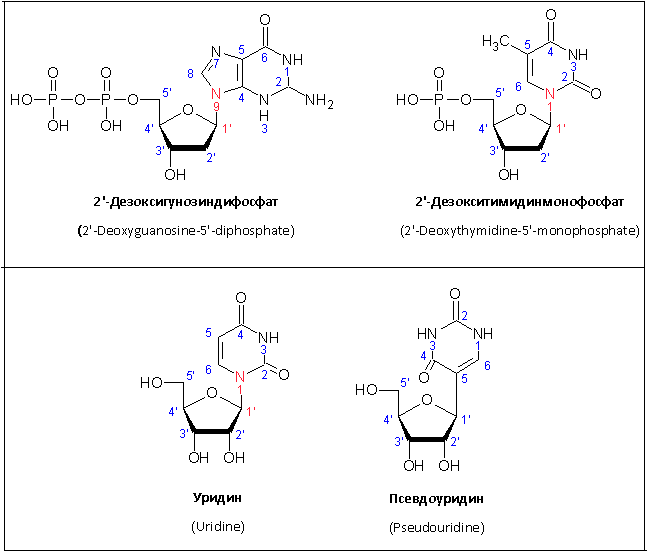

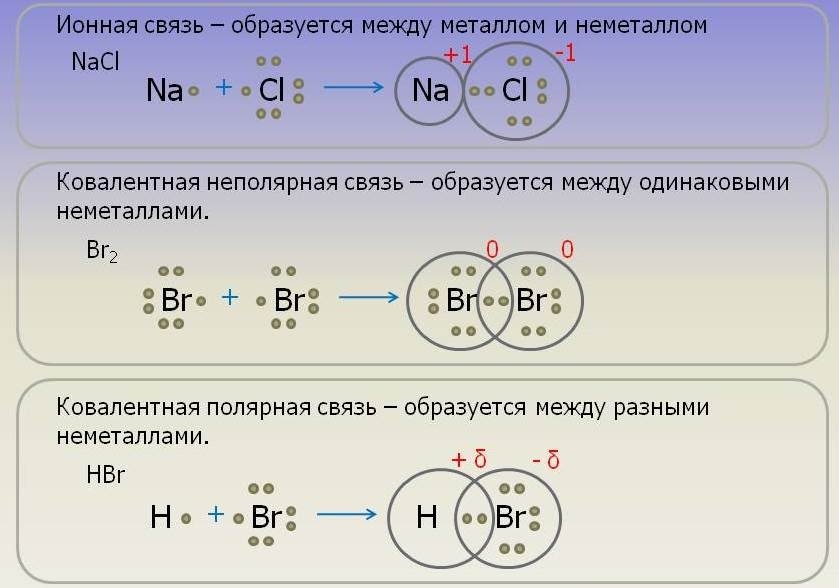
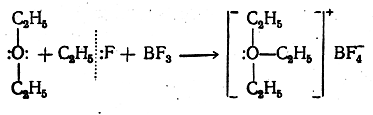
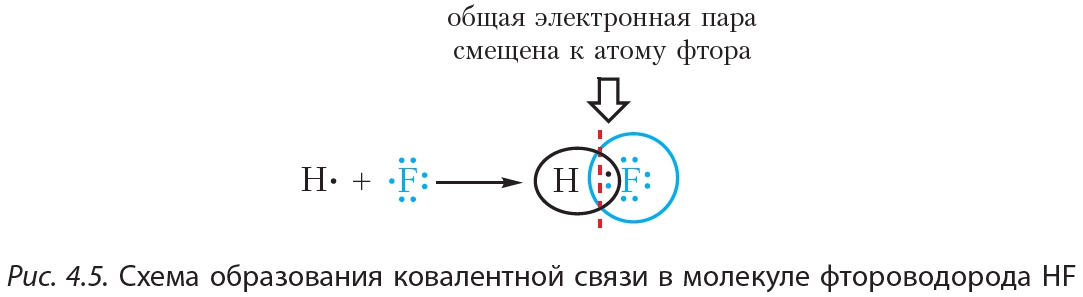
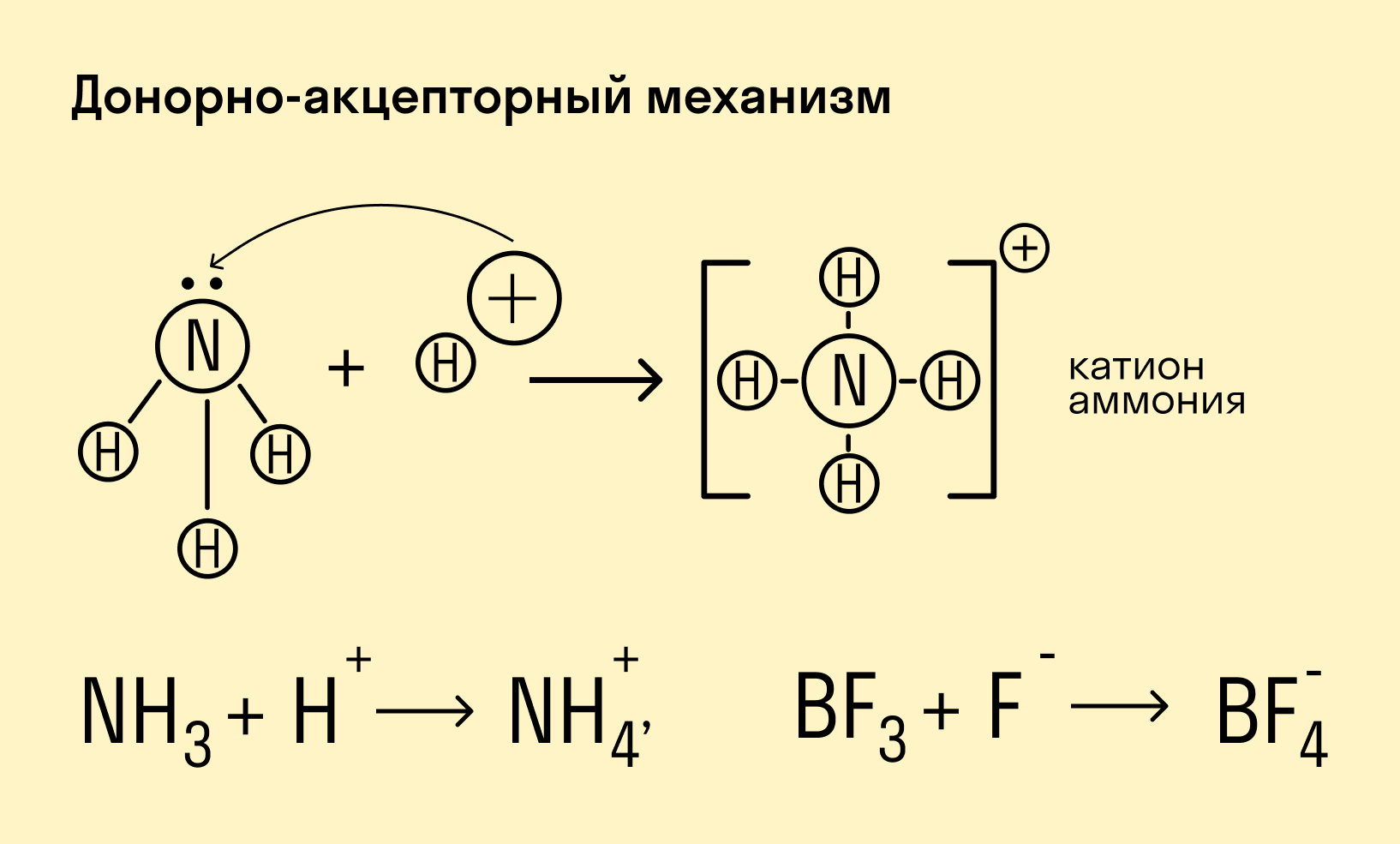
Атомы углерода могут быть связаны между собой не только одинарными, но и двойными связями. Простейшим углеводородом, содержащим двойную связь, является этилен. Рассмотрим строение его молекулы.