Дисперсные системы
Химическое взаимодействие в гомогенных реакций происходит при эффективных столкновениях активных частиц, а в гетерогенных — на поверхности раздела фаз при контакте реагирующих веществ, причем, скорость и механизм реакции зависят от площади поверхности, которая тем больше, чем сильнее развита поверхность. С этой точки зрения особый интерес представляют дисперсные системы, обладающие высокой удельной поверхностью. Дисперсная система — это смесь, состоящая как минимум из двух веществ, которые не реагируют друг с другом химически и обладают практически полной взаимной нерастворимостью. Дисперсная система - это система, в которой очень измельченные частички одного вещества равномерно распределены в объеме другого.

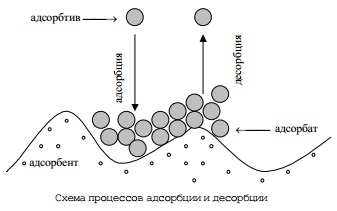

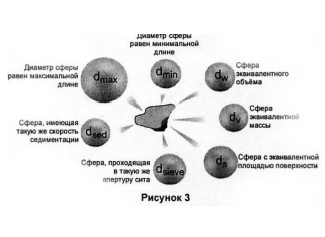

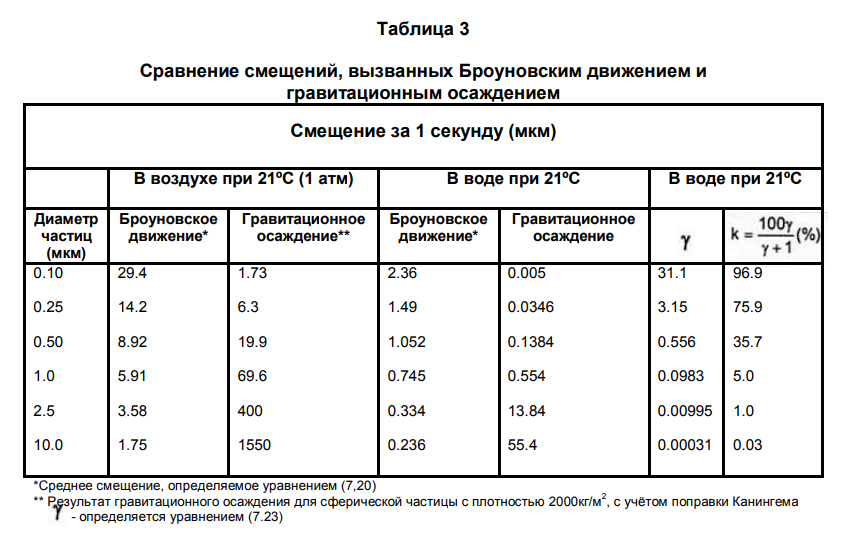



Условно различают грубо низко дисперсные системы с размером частиц от 1 мкм и выше и тонко высоко дисперсные системы с размером частиц ниже 1 мкм. Усредненным показателем дисперсности является удельная поверхность. Более полное представление о дисперсности дает кривая распределения объема или массы дисперсной фазы по размерам частиц. Для пористых тел вместо понятия дисперсности используют равнозначное понятие пористости.
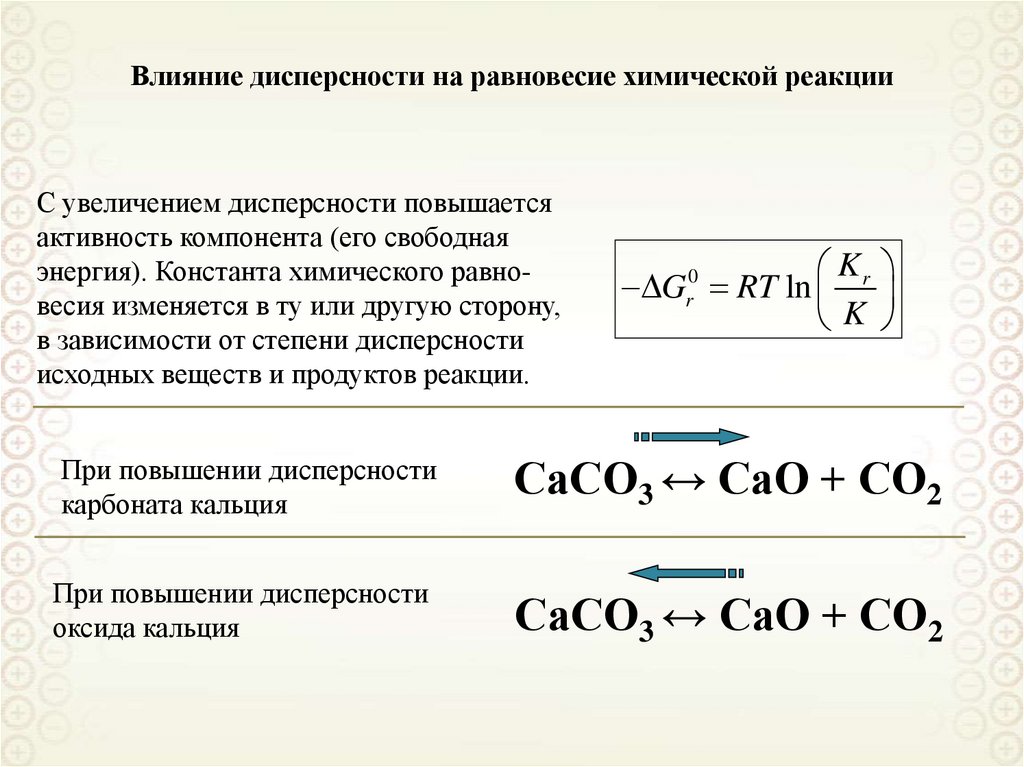


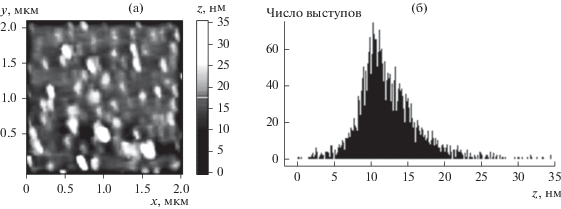


Дисперсность — физическая величина , характеризующая размер взвешенных частиц в дисперсных системах. Это величина, показывающая какое число частиц можно уложить вплотную в одном кубическом метре. Чем меньше размер частиц, тем больше дисперсность. Дисперсность имеет смысл отношения площади поверхности частиц к занимаемому ими объёму или к их суммарной массе. Условно различают грубо низко дисперсные системы с размером частиц от 1 мкм и выше и тонко высоко дисперсные системы с размером частиц ниже 1 мкм.