Масса и размер молекул
Атомы имеют очень маленький размер и очень маленькую массу. Если выражать массу атома какого-нибудь химического элемента в граммах, то это будет число, перед которым находится более двадцати нулей после запятой. Поэтому измерять массу атомов в граммах неудобно. Однако, если принять какую-либо очень малую массу за единицу, то все остальные малые массы можно выражать как отношение к этой единице. Это безразмерная величина, так как делятся две массы.
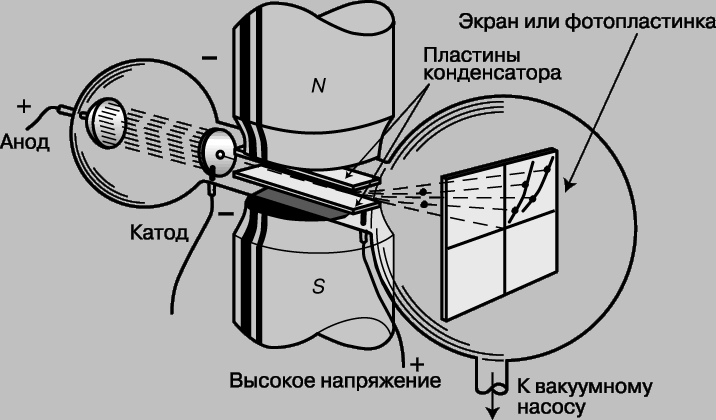

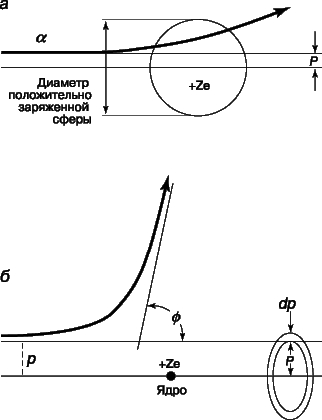
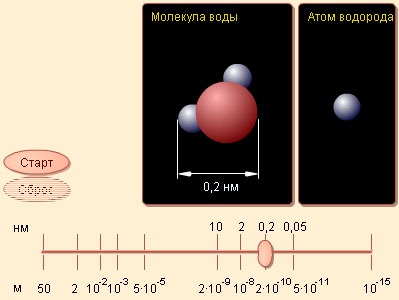



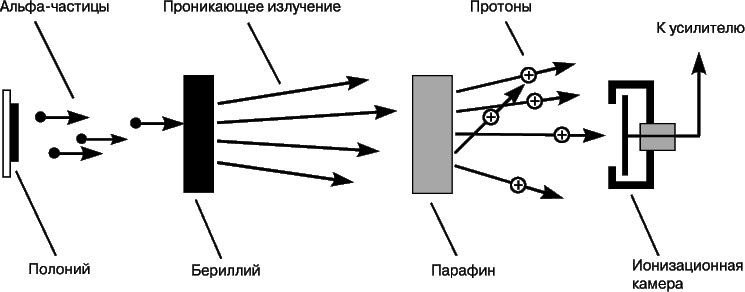
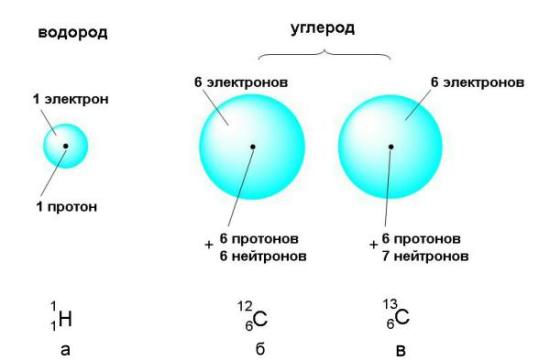
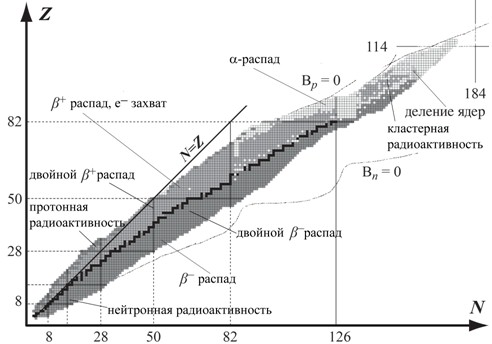
Атом состоит из ядра и окружающего его электронного "облака". Находящиеся в электронном облаке электроны несут отрицательный электрический заряд. Протоны , входящие в состав ядра, несут положительный заряд. В любом атоме число протонов в ядре в точности равно числу электронов в электронном облаке, поэтому атом в целом — нейтральная частица, не несущая заряда.
- Массы атомов чрезвычайно малы. Оперировать такими числами неудобно.
- Тестирование — это одна из форм проверки степени усвоения материала. Оно предоставляет возможность выявить пробелы в знаниях, скорректировать обучение и повысить его результативность на данном этапе.
- Атом - наименьшая составная часть вещества, сохраняющая его химические свойства. В обычных условиях атомы электронейтральны — число электронов в атоме равно числу протонов в атомном ядре.








Понятие об этой величине претерпевало длительные изменения в соответствии с изменением представления об атомах. Согласно теории Дальтона , все атомы одного и того же химического элемента идентичны и его атомная масса — это число, равное отношению их массы к массе атома некоего стандартного элемента. Однако примерно к стало ясно, что элементы, встречающиеся в природе, бывают двух типов: одни действительно представлены идентичными атомами, а у других атомы имеют одинаковый заряд ядра, но разную массу; такие разновидности атомов были названы изотопами. Определение Дальтона, таким образом, справедливо только для элементов первого типа. Атомная масса элемента, представленного несколькими изотопами, есть средняя величина из массовых чисел всех его изотопов, взятых в процентном отношении, отвечающем их распространенности в природе. В х годах было установлено, что природный кислород состоит из смеси трех изотопов: 16 О, 17 О и 18 О.